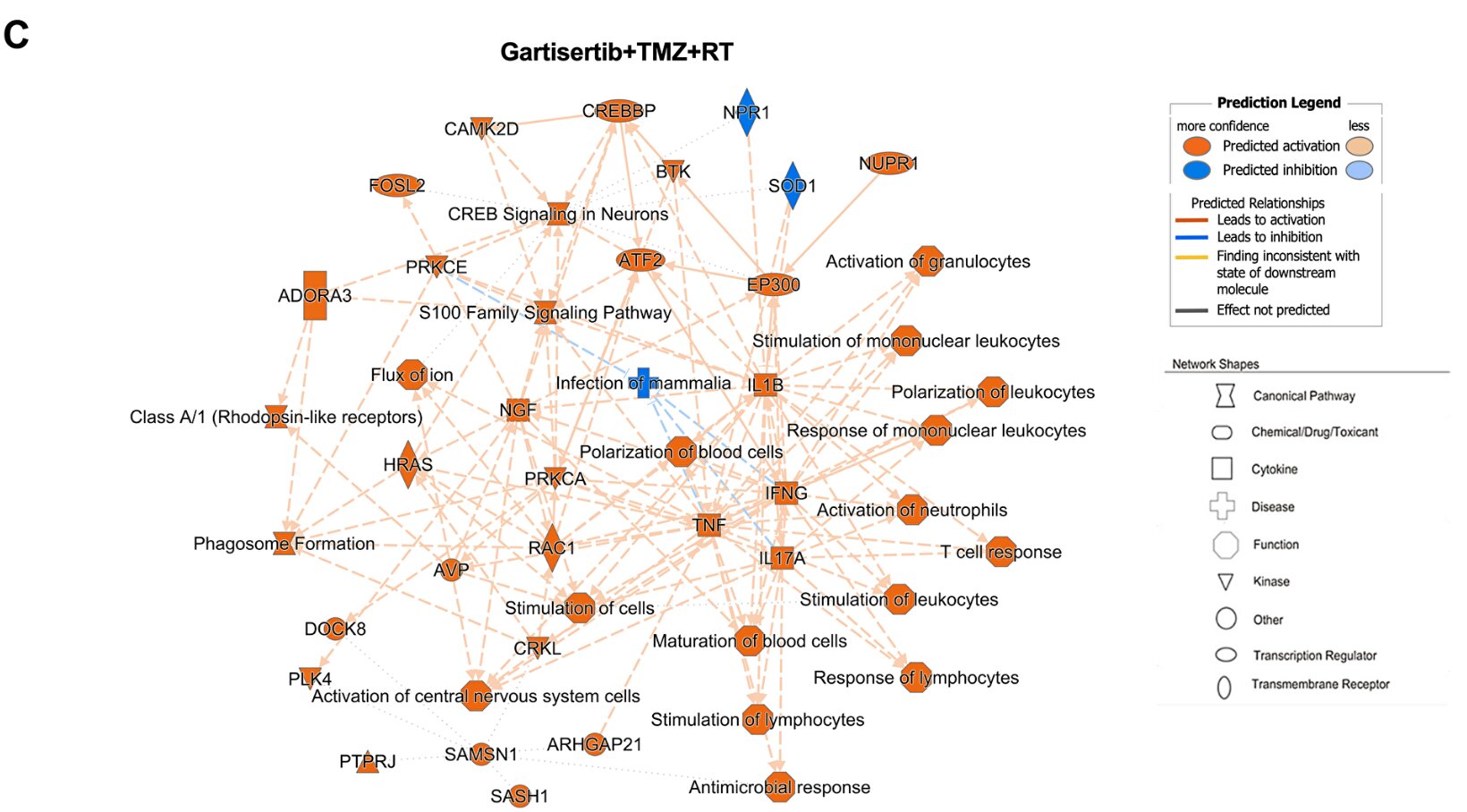
Zwiększona ekspresja genów i szlaków wzbogacona w linie komórkowe glejaka wielopostaciowego leczonych gartisertibem z TMZ+RT. kredyt: Oncotarget (2024). doi: 10.18632/oncotarget.28551
× Zamknąć
Zwiększona ekspresja genów i szlaków wzbogacona w linie komórkowe glejaka wielopostaciowego leczonych gartisertibem z TMZ+RT. kredyt: Oncotarget (2024). doi: 10.18632/oncotarget.28551
nowy Artykuł badawczy Został on opublikowany pod tytułem „Hamowanie ATR za pomocą gartesertybu zwiększa śmierć komórek i działa synergistycznie z temozolomidem i promieniowaniem w liniach komórkowych glejaka wielopostaciowego pochodzącego od pacjenta”. Oncotarget.
Komórki glejaka mogą ograniczać szkodliwe działanie temozolomidu (TMZ) i radioterapii (RT) na DNA, wykorzystując mechanizm reakcji na uszkodzenie DNA (DDR), który aktywuje zatrzymanie cyklu komórkowego i szlaki naprawy DNA. Ataksja-teleangiektazja i białko związane z Rad3 (ATR) odgrywają kluczową rolę w rozpoznawaniu uszkodzeń DNA wywołanych chemioterapią i promieniowaniem, które powodują aktywację DDR.
W nowym badaniu naukowcy Matthew Lozinski i Nicola A. Bowdena i Moiry C. Graves, Michael Fay, Brian W. Day, Brett W. Stringer i Paul A. Tony z Newcastle University, Hunter Medical Research Institute, GenesisCare i QIMR. Instytut Badań Medycznych Berghofera i Uniwersytet Griffith badały aktywność inhibitora ATR, gartesertybu, samego oraz w połączeniu z TMZ i/lub RT, w liniach komórkowych glejaka wielopostaciowego pochodzących od pacjentów.
„Korzystając z panelu 12 linii komórkowych glejaka wielopostaciowego pochodzących od pacjentów, badaliśmy działanie gartisertybu na chemio- i radiosensybilizację, silnego i selektywnego inhibitora ATR badanego w I fazie badania klinicznego u pacjentów z zaawansowanymi guzami litymi (NCT02278250).” Naukowcy wyjaśnić.
Zespół wykazał, że sam gartesertib skutecznie zmniejszał żywotność komórek w liniach komórkowych glejaka wielopostaciowego, gdzie wrażliwość była powiązana z częstszymi mutacjami DDR i wyższą ekspresją szlaku cyklu komórkowego G2. Hamowanie ATR znacząco zwiększało śmierć komórek w połączeniu z TMZ i RT i wykazano, że ma wyższą synergię niż leczenie TMZ + RT. Niemetylowane komórki glejaka wielopostaciowego oporne na TMZ+RT z promotorem MGMT były również bardziej wrażliwe na gartisertib. Analiza ekspresji genów w komórkach glejaka wielopostaciowego leczonych gartisertibem pozwoliła zidentyfikować regulację wrodzonych szlaków związanych z odpornością.
„Ogólnie rzecz biorąc, badanie to identyfikuje hamowanie ATR jako strategię mającą na celu zwiększenie zdolności standardowej terapii glejaka wielopostaciowego do uszkadzania DNA, dostarczając jednocześnie wstępnych dowodów na to, że hamowanie ATR indukuje sygnaturę genu wrodzonej odporności, która uzasadnia dalsze badania” – podsumowali naukowcy.
więcej informacji:
Matthew Losinski i wsp., hamowanie ATR za pomocą gartesertybu wzmaga śmierć komórek i działa synergicznie z temozolomidem i promieniowaniem w liniach komórkowych glejaka wielopostaciowego pochodzącego od pacjenta, Oncotarget (2024). doi: 10.18632/oncotarget.28551
Dostarczone przez Impact Journals LLC

„Chcę być miłośnikiem telewizji. Certyfikowany entuzjasta popkultury. Stypendysta Twittera. Student amator.”






More Stories
TRUE NORTH uruchomiła nową platformę marki „Life’s Different After” w ramach kampanii Today the Brave
Pomiar mowy ciała Wiadomości o Mirażu
W trakcie testu | Rower Giant Revolt 2025 ma dodatkowe schowki w dolnej rurze i twierdzi, że zapewnia większy komfort